Série « MYTHES » : Le pH de l'eau est lié au pH du substrat

Le pH est une mesure des ions d'hydrogène (H+) et des ions d'hydroxyde (OH-) d'une solution comme l'eau. L'intervalle de pH est de ‘0’ (très acide : la concentration d'ions H+ est plus élevée que la concentration de OH-) à ‘14’ (très basique : la concentration d'ions OH- est plus élevée que la concentration de H+). Lorsque le pH est de 7, il est neutre, ce qui signifie que la concentration de H+ et de OH- est la même. Le pH de l'eau est important lorsque l'on souhaite y ajouter des pesticides ou dissoudre des micronutriments. Toutefois, le pH de l'eau a peu d'influence sur le pH du substrat. Tel qu'expliqué ci-dessous, d'autres facteurs ont un impact sur le pH d'un substrat.
Alcalinité de l'eau
Le pH de l'eau d'irrigation n'est pas aussi important que son alcalinité (CaCO3) lorsqu'on travaille avec des substrats non inertes comme la tourbe de sphaigne. L'alcalinité est une mesure de la quantité de carbonates et/ou de bicarbonates, ou plus simplement de la quantité de chaux dissoute dans l'eau d'irrigation. Lorsque l'alcalinité de l'eau est élevée, cela veut dire qu'elle contient une grande quantité de chaux. Avec chaque arrosage, de la chaux est ajoutée au substrat, ce qui entraîne une augmentation de son pH avec le temps (Figure 1). De plus, l'eau ayant une alcalinité élevée a une grande capacité de tamponnage en comparaison à l'eau ayant une faible alcalinité. La capacité de tamponnage est la capacité de résister aux changements. Par conséquent, plus cette capacité est grande, plus la résistance aux changements et la capacité de réduire le pH de l'eau sont élevées.
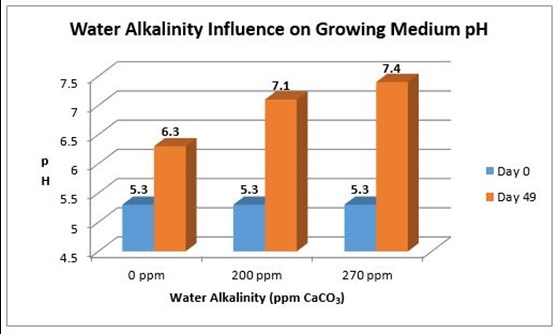
Il y a des intervalles pour une alcalinité optimale pour différentes grosseurs de contenants:
- Plantules : 60-100 ppm CaCO3
- Petits pots (4” ou moins), plateaux de culture : 80-140 ppm CaCO3
- Grands pots (>4”), cultures à long terme : 120-180 ppm CaCO3
La principale différence entre ces intervalles est le lien avec le taux d'application d'engrais et la taille du plant pour chaque grosseur de contenant. L'effet d'un engrais acide sur une petite plantule sera négligeable puisque le taux serait bas et que la plante est très petite en comparaison avec le taux d'un grand pot (voir discussion dans la section « Engrais »).
Prenons un producteur de plantules qui utilise le même substrat à base de tourbe de sphaigne pour cultiver à deux endroits différents. Dans les deux cas, le producteur arrose ses cultures avec de l'eau de puits ayant un pH de 8. L'alcalinité de l'eau est de 300 ppm CaCO3 au premier endroit, et de 150 ppm CaCO3 au deuxième. Sur la base de l'intervalle normal de 60-100 ppm CaCO3, nous pouvons conclure que l'alcalinité de chacune des sources d'eau est élevée et que de l'acide doit être injecté pour la réduire. Dans ce cas-ci, 80 ppm CaCO3 sera l'objectif. Les résultats apparaissent au Tableau 1.
| Endroit | pH de départ | Alcalinité de l'eau | once liquide/gallon acide sulfurique* pour réduire l'alcalinité à 80 ppm | pH final |
|---|---|---|---|---|
| 1 | 8 | 300 | 6.27 | 5.9 |
| 2 | 8 | 150 | 2.02 | 6.4 |
Notez que la quantité d'acide sulfurique requise pour réduire l'alcalinité à 80 ppm CaCO3 et le pH subséquent a été basée sur l'alcalinité de l'eau et non sur son pH.
Engrais
Pendant l'absorption d'engrais, les plantes émettent de l'hydrogène et des ions d'hydroxyle/bicarbonate dans le substrat, ce qui a pour effet de changer le pH du substrat. Généralement, plus la plante est grosse, plus la quantité d'engrais utilisée est grande, et plus la plante est rapide à changer le pH du substrat. Tous les éléments contenus dans les engrais, et spécialement l'azote, vont soit réduire ou augmenter le pH du substrat. L'azote est disponible sous trois formes différentes : nitrate, ammonium et urée. Le nitrate (NO3-) a une charge négative, l'ammonium (NH4+) a une charge positive, et l'urée (CO(NH2)2) n'a pas de charge du tout. Lorsque les racines des plantes absorbent du nitrate (chargé négativement), elles libèrent du OH- ou du bicarbonate (HCO3-) afin de maintenir l'équilibre électrique. Lorsque les plantes absorbent de l'ammonium (chargé positivement) les racines libèrent du H+ pour équilibrer les charges à l'intérieur de la plante. Enfin, l'urée doit être transformée en ammonium pour être absorbée par les plantes. Avec l'aide des bactéries, l'urée peut être transformée d'abord en ammoniac, et ensuite en nitrate. Ce processus de transformation de l'ammonium en nitrate est appelé « nitrification ».
Les engrais contenant une grande quantité d'azote ammoniacal, comme le 20-20-20, ont l'acidité potentielle pour neutraliser 576 lb de carbonate de calcium pour chaque tonne d'engrais absorbé par une culture ou, en d'autres mots, pour réduire le pH du substrat. Les engrais contenant une grande quantité d'azote des nitrates, comme le 15-5-15 Cal-Mag, ont pour effet d'ajouter 131 lb de carbonate de calcium (chaux) pour chaque tonne d'engrais utilisé par la plante ou, en d'autres mots, pour augmenter le pH du substrat. En choisissant des engrais potentiellement acides ou basiques sur la base de la source d'azote, le pH du substrat peut être maintenu dans les intervalles optimaux.
Il est extrêmement important de surveiller la fertilisation lorsqu'on utilise de l'eau ayant une faible alcalinité (<40 ppm CaCO3) pour arroser les plantes. L'eau ayant une faible alcalinité a une capacité de tamponnage limitée. Par conséquent, l'application d'engrais potentiellement acides peut avoir un impact énorme sur le pH du substrat. Dans un tel cas, un engrais potentiellement acide pourrait faire chuter le pH du substrat à un niveau inacceptable. Le même principe s'applique à l'eau obtenue par osmose inversée puisque l'alcalinité de l'eau traitée peut être extrêmement basse.
Le pH du substrat est important parce qu'il détermine la disponibilité des nutriments. Par exemple, la disponibilité des micronutriments comme le fer, le manganèse, le zinc et le cuivre augmente lorsque le pH est en-dessous de 5.5. D'un autre côté, la disponibilité du molybdène, du calcium et du magnésium diminue. L'inverse se produit à des pH supérieurs à 6.5. Sur la base de ces faits, nous recommandons de maintenir le pH du substrat entre 5.5 et 6.5.
Espèces végétales
Même si cela n'est pas aussi significatif, certaines espèces de plantes influencent également le pH des substrats. Par exemple, le zinnia et le vinca ont tendance à faire augmenter le pH du substrat avec le temps, les pensées n'ont aucun effet sur le pH des substrats, et les tomates, le dianthus et la célosie ont tendance à faire baisser le pH du substrat.
En conclusion, il est très important de vérifier l'alcalinité de l'eau avant le début de chaque saison. En connaissant l'alcalinité de l'eau, un producteur est en mesure de prendre de meilleures décisions en matière de fertilisation afin de maintenir le pH du substrat dans les intervalles optimaux.